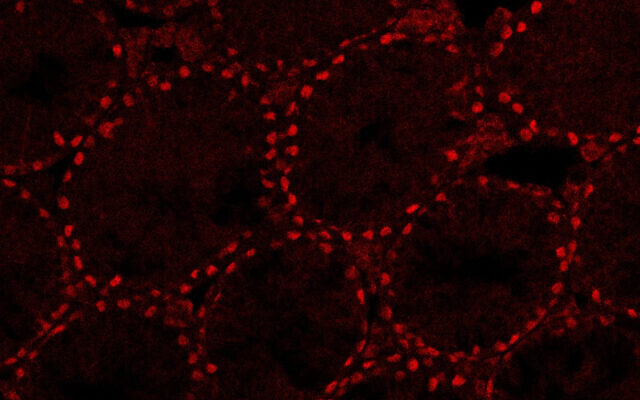
En una primicia científica, investigadores de la Universidad de Bar-Ilan han creado testículos en un laboratorio, un descubrimiento que esperan que pueda conducir a una mejor comprensión de la determinación del sexo, así como a avances en el tratamiento de la infertilidad.
Los «testículos de laboratorio» no son de tamaño natural, sino organoides, que son versiones tridimensionales en miniatura y simplificadas producidas in vitro que imitan las funciones biológicas clave y las estructuras de un órgano.
El nuevo logro se publicó recientemente como un estudio revisado por pares en el International Journal of Biological Studies.
«Este último estudio surge del enfoque de mi laboratorio en el proceso de determinación del sexo y el desarrollo de las gónadas, que son los testículos en los hombres y los ovarios en las mujeres. Hemos estado investigando los trastornos del desarrollo sexual [antes conocidos como intersexuales], que ocurren en 1 de cada 4,000 nacimientos», dijo el investigador principal, el Dr. Nitzan Gonen.
Hasta ahora, no había más remedio que estudiar la determinación del sexo in vivo, principalmente con ratones. Se trata de un proceso largo y complejo que implica la edición del genoma, la producción de ratones con mutaciones genéticas y su posterior apertura en un momento determinado de su desarrollo para examinar sus gónadas.
Obtenga la edición diaria de The Times of Israelpor correo electrónico y nunca te pierdas nuestras mejores historiasDirección de correo electrónico del boletínCONSÍGUELOAl registrarse, acepta los términos
«Entonces, para comprender mejor los trastornos del desarrollo sexual y cómo se desarrollan y funcionan las gónadas en general, sabíamos que sería extremadamente útil para nosotros tener un sistema in vitro en el laboratorio. Queríamos tener un modelo de los testículos en una placa que tuviera muchas células en las que pudiéramos insertar mutaciones y cosechar células para todo tipo de experimentos», dijo Gonen.
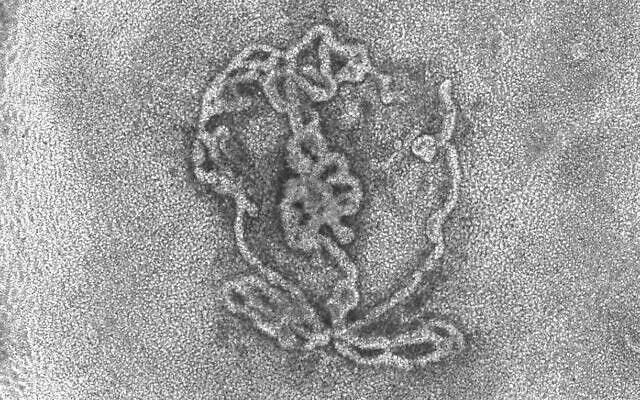
Si bien los científicos ya han logrado avances significativos en el desarrollo de organoides reproductivos femeninos, hasta ahora no hay avances paralelos para los testículos, que son responsables de producir espermatozoides y hormonas sexuales masculinas como la testosterona.
Por lo tanto, el objetivo era crear un organoide con los tres tipos de células que se encuentran en los testículos. Las primeras son las células germinales, que dan lugar a los espermatozoides. Las otras son las células de Sertoli, que nutren a las células germinales para que puedan producir espermatozoides, y las células de Leydig, que secretan testosterona.
Inicialmente, Gonen y su equipo tomaron células madre embrionarias y lograron convertirlas en células testicular en etapa temprana a través de un proceso llamado biología regenerativa. Sin embargo, hubo un fallo.
«Me di cuenta de que si tomaba estas células gonadales tan tempranas y las ponía en un plato estándar con medios básicos, no podría mantenerlas. Así que este enfoque de generar las células gonadales a partir de células madre no me ayudaría», dijo Gonen.

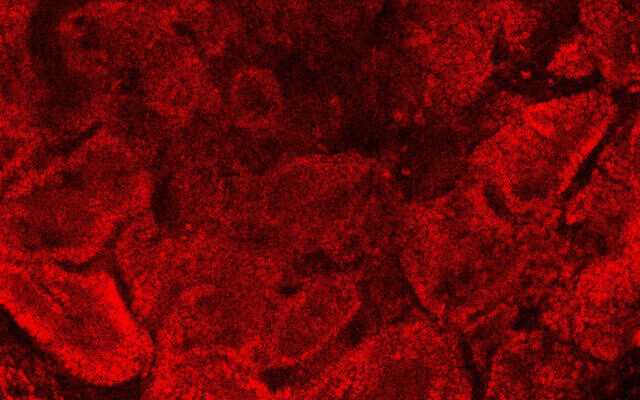
El siguiente paso, en el que se centró el estudio recién publicado, fue tomar testículos de crías de ratones de tres a cuatro días de edad y disociarlos en células individuales. A través de un proceso de prueba y error de diferentes técnicas, Gonen y su equipo lograron convertirlos en organoides de testículos repletos de las estructuras adecuadas de células germinales, células de Sertoli y células de Leydig.
Descubrieron que cuanto más jóvenes eran los cachorros, mejor podían crecer sus células en «testículos de laboratorio».
«Pudimos conservarlos durante un período de nueve semanas, que es mucho tiempo y algo que nadie ha podido hacer antes», declaró Gonen.
«Verificamos la expresión de todos los diferentes marcadores de las células durante esas nueve semanas y vimos que eran muy similares a cómo se expresan las cosas en los testículos reales», dijo.
Según Gonen, este período de nueve semanas es teóricamente lo suficientemente largo como para que los testículos comiencen la espermatogénesis (la creación de espermatozoides). Dijo que vio señales iniciales de esto, pero que se necesitan más estudios para asegurarse de que esto está ocurriendo.
«Teóricamente, el proceso de espermatogénesis debería durar 34 días en ratones. Así que tal vez haya células dentro de eso que ya lo hayan hecho y aún no lo sabemos. Estamos trabajando en eso ahora», declaró Gonen.
Gonen compartió que está ansiosa por hacer avanzar la investigación de los ratones a los humanos para que se puedan abordar los problemas de infertilidad.
En una posible aplicación, anotó, algunos chicos tienen cáncer y deben someterse a tratamientos de quimioterapia que destruyen las células madre de los testículos que se convierten en espermatozoides en la pubertad.
En Israel y otros países, a este niño prepúber y a sus padres se les da la opción de que el niño se someta a un procedimiento laparoscópico para extraer una biopsia de tejido testicular. Esta biopsia se divide en rodajas y se congela. Sin embargo, en este punto, no hay nada que se pueda hacer para generar espermatozoides a partir de esas células.
En un intento por ayudar a estos niños a ser capaces de engendrar biológicamente hijos, Gonen está trabajando con un médico del Centro Médico Hadassah que está proporcionando a su laboratorio algunas rebanadas de estas muestras congeladas.
«Intentaremos hacer más o menos lo mismo con las células gonadales de estos niños que hicimos con las células de los cachorros de ratones. Disociaremos las células de los testículos y las reconstruiremos para ver si podemos generar organoides de testículos humanos que funcionen como deberían en términos de producción de espermatozoides», dijo Gonen.
También quiere ver si puede ayudar a los hombres adultos con infertilidad, señalando sin embargo que se necesitaría un enfoque diferente, ya que solo tuvo éxito en la creación de «testículos de laboratorio» a partir de crías de ratón y ratones prenatales. Cuando su equipo probó el método en ratones mayores, no funcionó debido a los cambios que experimentan los testículos durante la pubertad.
Gonen cree que la solución puede ser tomar células somáticas, como las células de la piel, de hombres adultos y revertirlas en células madre pluripotentes inducidas y cultivarlas.
«La esperanza sería que los organoides testículos resultantes fueran más resistentes y sobrevivieran más tiempo que los cultivados a partir de células madre embrionarias y que produjeran espermatozoides para la fertilización in vitro de un óvulo humano», dijo.